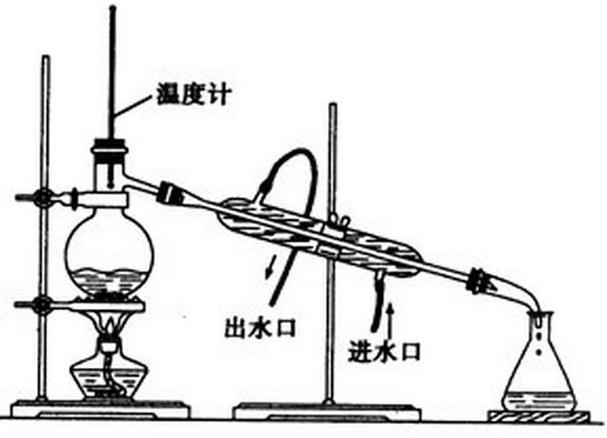
共沸物如何分離:打破混合物極限的實用解析
Table of Contents
共沸物如何分離:打破混合物極限的實用解析
您是否曾經在實驗室或生產線上,面對著兩種原本可以輕鬆蒸餾分離的液體,卻發現它們在混合後,蒸餾到某個特定比例時,就一同沸騰,無法再進一步分離?這時候,您遇到的很可能就是「共沸物」。共沸物,簡單來說,就是一種特殊的混合物,它在特定的溫度下,會以固定的比例一同蒸發,且氣相與液相的組成相同。這使得傳統的簡單蒸餾方法,對它們束手無策。別擔心,這可不是什麼無法克服的難題!透過一些巧妙的化學工程與物理原理,我們有辦法「打破」共沸的限制,達成更純粹的分離目標。接下來,就讓我們一起深入探討,共沸物到底是如何被分離的吧!
共沸現象的迷人面紗:為什麼會發生?
要理解如何分離共沸物,首先得弄懂它為什麼會產生。這得從「溶液的蒸氣壓」說起。一般情況下,理想溶液中的組分蒸氣壓會遵循拉午耳定律(Raoult’s Law),也就是說,混合物的總蒸氣壓等於各組分純蒸氣壓的加權平均。然而,現實中的許多溶液,尤其是某些極性相近或能形成氫鍵的液體,會表現出「非理想性」。
非理想溶液大致分為兩類:
- 正偏差溶液:組分之間的吸引力比組分與自身之間的吸引力弱,導致蒸氣壓比理想溶液高,有形成「最小沸點共沸物」的傾向。
- 負偏差溶液:組分之間的吸引力比組分與自身之間的吸引力強,導致蒸氣壓比理想溶液低,有形成「最大沸點共沸物」的傾向。
當溶液的蒸氣壓達到一個極值(最大或最小),並且在此極值點上,氣相和液相的組成恰好相同時,就形成了共沸點。這意味著,在這個特定比例下,無論您怎麼加熱,蒸發出來的蒸汽濃度和殘留在鍋裡的液體濃度都一模一樣,根本無法透過蒸餾得到純物質。
以最常見的乙醇-水體系為例,乙醇和水混合後,會形成一個最小沸點共沸物,約為95.6%的乙醇(重量百分比)在78.2°C沸騰。即使您不斷蒸餾,最終留在瓶裡的,也只會是這種約95.6%的乙醇水溶液,無法得到100%的純乙醇。
如何「動手腳」打破共沸?
既然簡單蒸餾不行,我們就得祭出一些「進階」的招數了!這些方法的核心思想,都是要麼改變體系的壓力,要麼引入「第三方」,讓原來的共沸點「消失」或「移動」,進而創造出分離的機會。
打破共沸的實戰策略
接下來,我們將介紹幾種最常見且有效的共沸物分離方法,這些方法在化學工業中扮演著舉足輕重的角色。
1. 壓力變動蒸餾法 (Pressure Swing Distillation, PSD)
您知道嗎?共沸點的溫度和組成,是會受到壓力影響的!有些共沸物的組成會隨著壓力變化而改變。壓力變動蒸餾法,就是利用這個特性來達到分離的目的。
這個方法通常需要兩套蒸餾塔,一套在高壓下操作,另一套在低壓下操作。
- 第一階段 (高壓塔):將含有共沸物的混合物送入高壓蒸餾塔。在高壓下,原來的共沸物組成會發生改變,例如,原本在常壓下形成共沸的比例,在高壓下可能不再是共沸點,我們可以從塔頂得到一種較純的組分,而塔底則是另一種較純的組分,但其中一種組分可能還含有較多的另一種雜質。
- 第二階段 (低壓塔):將第一階段蒸餾得到的、含有雜質的較純組分,送入低壓蒸餾塔進行再次蒸餾。在低壓下,共沸物的比例又會發生變化,進一步將兩種組分分離開。
透過在高低不同壓力下反覆操作,我們就能逐步提高目標組分的純度。這種方法特別適用於那些共沸組成隨壓力變化明顯的體系,例如乙醇-水系統。
2. 共沸蒸餾法 (Azeotropic Distillation)
這是一種非常「聰明」的方法,我們巧妙地引入一個「夾帶劑」(entrainer)。夾帶劑是一種能夠與混合物中的一個或多個組分形成新的、低沸點的共沸物,或者改變原有的共沸組成,從而將原來的共沸物「打散」。
操作步驟大致如下:
- 加入夾帶劑:將適當的夾帶劑加入原共沸物中。夾帶劑的選擇至關重要,它需要能與目標組分(或雜質組分)形成易於蒸出的新共沸物,並且其自身與另一組分不形成難以分離的共沸物。
- 形成新共沸物:加入夾帶劑後,原有的共沸關係被打破。通常,夾帶劑會與混合物中的某種成分形成一個新的、沸點更低的共沸物。
- 蒸餾分離:這個新的、低沸點的共沸物會優先被蒸餾出來。通過冷凝後,又分為兩相(例如,水相和有機相),便於將其分離。
- 回收夾帶劑:分離出來的夾帶劑,通常會被回收並循環使用,以降低成本。
例如,要分離乙醇-水共沸物,常常會加入苯、環己烷或氯仿作為夾帶劑。以苯為例,苯會與乙醇形成一個低沸點的共沸物,一起蒸出。冷凝後,由於苯和水的溶解度不同,會形成兩層:一層是含乙醇和苯的有機層,另一層是較純的水。我們可以將這兩層分開,再進行後續處理,最終得到較純的乙醇。
我的經驗是,選擇一個好的夾帶劑,就像為了一場硬仗找到一個關鍵的盟友,能讓整個分離過程事半功倍。但同時,夾帶劑的回收和處理也需要仔細考量,以免造成二次污染或成本增加。
3. 萃取蒸餾法 (Extractive Distillation)
萃取蒸餾法與共沸蒸餾法有些相似,同樣是引入一個「萃取劑」(solvent),但它的作用方式略有不同。在這個方法中,萃取劑的沸點比混合物中的任何一種組分都要高,因此它不會一同蒸發,而是留在蒸餾塔的底部。
操作過程如下:
- 引入高沸點萃取劑:將高沸點的萃取劑從蒸餾塔頂部加入。
- 改變相對揮發度:萃取劑與混合物中的某一組分(通常是較難分離的組分)產生較強的相互作用,改變了其蒸氣壓和揮發度。這樣一來,原來難以分離的組分,其相對揮發度就變大了。
- 蒸餾分離:在蒸餾塔中,沸點較低的組分(雜質)會先被蒸出,而目標組分則在高沸點萃取劑的作用下,傾向於留在塔底。
- 回收萃取劑:從塔底得到的混合物(目標組分與萃取劑),再透過另一個蒸餾塔或萃取操作,將目標組分與萃取劑分離,並回收萃取劑。
例如,在分離丁二烯(一種烯烴)和丁烷(一種烷烴)的過程中,由於它們沸點接近,且容易形成共沸,常常會使用乙腈或二甲基甲酰胺(DMF)等作為萃取劑。這些極性溶劑與丁二烯的相互作用比丁烷強,從而提高丁二烯的揮發度,使其更容易與丁烷分離。
我個人認為,萃取蒸餾法的關鍵在於選擇一個能夠與目標組分產生足夠大揮發度差異的萃取劑,同時這個萃取劑又不能與其他組分產生新的難以分離的共沸物,這對技術的要求相當高。
4. 膜分離技術 (Membrane Separation)
除了傳統的蒸餾方法,現代科學技術還帶來了更多創新的解決方案,其中膜分離技術就展現出巨大的潛力。這類技術利用特殊的「膜」,根據分子大小、親和力或溶解度等差異,來實現組分的選擇性透過。
常見的膜分離技術包括:
- 滲透蒸發 (Pervaporation):這是一種利用膜來分離液體混合物的技術。膜具有選擇性,只允許特定組分(例如水)滲透通過,而另一組分(例如乙醇)則被截留。滲透蒸發通常需要藉助真空或溫度梯度來推動滲透過程。
- 納濾 (Nanofiltration):納濾膜的孔徑介於超濾和反滲透之間,能夠有效截留分子量較大的溶質,同時允許溶劑通過。
以滲透蒸壓分離乙醇-水共沸物為例,選擇一種對水具有高選擇性的親水性膜。當共沸物流過膜的一側時,水分子會優先透過膜,而較難透過的乙醇則被濃縮在膜的另一側。這種方法的好處是能耗較低,且操作條件溫和,但膜的壽命和通量是需要考慮的關鍵因素。
5. 吸附法 (Adsorption)
吸附法是利用固體吸附劑對混合物中不同組分具有不同吸附能力的原理來進行分離。某些吸附劑,如分子篩(zeolites),它們的孔徑大小和表面化學性質,可以選擇性地吸附混合物中的某種成分。
以分離乙醇-水共沸物為例,可以選用一種對水具有強親和力的分子篩。當共沸物通過填充有這種分子篩的吸附柱時,水分子會被牢牢吸附在分子篩的孔隙中,而乙醇則得以透過。當吸附劑達到飽和後,可以透過升溫或降低壓力等方式將吸附的組分「解吸」,從而得到較純的組分。
這種方法同樣適用於處理對壓力或溫度敏感的物質。不過,吸附劑的再生和壽命,以及吸附容量,是需要仔細評估的。
總結:策略性的挑戰,智慧性的解決
共沸物的形成,無疑為化學分離帶來了「看似」無法跨越的障礙。然而,從壓力變動蒸餾、共沸蒸餾、萃取蒸餾,到現代的膜分離和吸附技術,我們已經發展出多樣且有效的手段來應對這個挑戰。每一次的分離方法的選擇,都像是在進行一場「策略遊戲」,需要深入了解物質本身的特性,以及各種分離技術的原理與優缺點。
我認為,共沸物分離的智慧,不僅僅在於掌握這些複雜的工程技術,更在於對物質世界細微差異的洞察與運用。透過不斷的研發與創新,我們總能找到那把「鑰匙」,開啟共沸物緊鎖的秘密,讓純粹的化學物質得以重現。
常見問題與詳盡解答
問:為什麼我簡單蒸餾出來的乙醇純度最高只能到95.6%?
答:這正是因為乙醇和水形成了一個「最小沸點共沸物」。在約95.6%(重量百分比)的乙醇濃度下,乙醇和水的混合物會在78.2°C同時沸騰,而且蒸氣和液體的組成是相同的。這意味著,當您不斷加熱蒸餾時,蒸發出來的蒸汽仍然是95.6%的乙醇,殘留在鍋裡的液體也是95.6%的乙醇。因此,簡單蒸餾無法突破這個共沸點,得到更高純度的乙醇。
問:共沸蒸餾法中的「夾帶劑」選擇標準是什麼?
答:選擇夾帶劑的標準需要非常嚴謹。首先,夾帶劑必須能夠與混合物中的一個或兩個組分形成一個新的、沸點比原共沸物更低的共沸物,這樣才能讓它優先蒸出。其次,夾帶劑與目標組分(或雜質組分)之間的相互作用,應該能夠有效地改變它們的相對揮發度,打破原來的共沸關係。此外,夾帶劑本身不應該與另一組分形成難以處理的共沸物,並且最好能夠方便地從蒸出的混合物中回收和再利用,以降低成本和減少環境影響。例如,對於乙醇-水系統,苯、環己烷、氯仿等都是常用的夾帶劑,它們與乙醇形成低沸點共沸物的能力,以及其後續分離的便利性,都是選擇的考量因素。
問:壓力變動蒸餾法聽起來很複雜,實際操作中會不會很難?
答:壓力變動蒸餾法的確比單純的簡單蒸餾複雜,因為它涉及到多個壓力下的操作,需要更精密的設備控制。這通常需要兩套或更多套蒸餾塔,分別在高壓和低壓下運行,並有相應的壓力調節和物料轉移系統。然而,對於需要獲得極高純度組分的工業生產來說,這種複雜性是值得的。許多大型化工廠,例如生產無水乙醇的廠家,就廣泛使用壓力變動蒸餾法。透過精密的自動化控制系統,操作上的難度可以得到很好的管理。
問:膜分離技術和傳統蒸餾法相比,有哪些優勢和劣勢?
答:膜分離技術相較於傳統蒸餾法,有幾個顯著的優勢。首先,它的能耗通常較低,因為它不一定需要進行劇烈的加熱和冷卻過程,特別是滲透蒸發。其次,操作條件相對溫和,對於熱敏感的物質比較友好。再者,膜分離設備相對緊湊,佔地面積較小。然而,膜分離技術也有其劣勢。最主要的是膜的壽命和選擇性,膜可能會受到化學物質的腐蝕、堵塞,或者在長時間運行後性能下降,需要定期更換,這會增加運營成本。此外,對於某些複雜的混合物,單一的膜分離技術可能無法達到所需的分離度,需要與其他技術結合使用。
問:我聽說利用分子篩可以吸附水。那是不是說,只要我把含水的乙醇和分子篩放在一起,就能得到純乙醇了?
答:理論上是這樣的,但實際上操作會更複雜一些。分子篩確實能選擇性地吸附水,這是因為某些分子篩的孔徑大小和表面化學性質,使其對水分子有較強的親和力。當您將乙醇-水共沸物通過填充有適當分子篩的吸附柱時,水會被吸附到分子篩的孔隙中,而較純的乙醇則可以流出。但是,吸附劑(分子篩)總有吸附飽和的時候。當它吸附了足夠多的水後,就無法再吸附更多的水了。因此,您需要一個「再生」的步驟,例如加熱分子篩,將吸附的水「脫附」出來,這樣分子篩才能被重複利用。這就形成了一個「吸附-脫附」的循環過程,而不是簡單的「放在一起」那麼直接。而且,要達到非常高的純度,可能需要多級吸附或結合其他分離方法。